Articolo – “Informazione Medico Scientifica e deposito dei Materiali promozionali in AIFA: l’esperienza delle Aziende”
Informazione Medico Scientifica e deposito dei Materiali promozionali in AIFA: l’esperienza delle Aziende
Maria Letizia Alessi (Merck Serono), Simona Largoni (Abbvie), Francesca Mongelli (Santen), Sveva Sanzone (Biogen)
- INTRODUZIONE
- MATERIALI E METODI
- SINTESI DEI RISULTATI
- CONSIDERAZIONI
- TIP AND TRICKS
- CONCLUSIONI
- INTRODUZIONE
Questo articolo riporta i risultati emersi da una survey condotta a cavallo tra il 2021 e il 2022 tra i partecipanti del gruppo di lavoro SIARV sull’informazione medico scientifica (GdL SIARV IMS, di seguito GdL), più specificatamente è stato richiesto di condividere le proprie esperienze relative alle pratiche di deposito dei materiali promozionali (MP) effettuate nel periodo 2020/2021.
Si evidenzia che la normativa che disciplina la pubblicità dei medicinali presso gli operatori sanitari è aggiornata al 2006 (Decreto Legislativo 24 aprile 2006, n. 219 e s.m.i – di seguito D.Lvo 219/06), anno in cui la maggior parte dei mezzi digitali, oggi diffusi e quotidianamente consultati, non esisteva.
A distanza di 15 anni dall’entrata in vigore di questo decreto sono state promulgate da AIFA alcune circolari esplicative ma la velocità di evoluzione dei mezzi di comunicazione è tale da richiedere uno sforzo costante per restare al passo con i tempi a beneficio dei professionisti di questo settore.
L’evoluzione della comunicazione è stata ulteriormente alimentata dalla pandemia di Covid-19 ed anche le aziende e gli operatori sanitari sono stati obbligati a sperimentare nuove forme di comunicazione.
I principi della normativa, che definiscono i requisiti che la pubblicità destinata all’operatore sanitario deve rispettare, sono elencati al titolo VIII del decreto sopra citato, in particolare agli art. 113, 119 e 120. In sintesi:
- gli operatori sanitari a cui può essere destinata la pubblicità di un medicinale sono le persone autorizzate a prescriverlo o a dispensarlo;
- la pubblicità deve sempre includere il Riassunto delle Caratteristiche del Prodotto (RCP) autorizzato, specificare la classificazione del medicinale ai fini della fornitura, il prezzo di vendita (ad eccezione dei casi previsti al c.4 Art.119) e le condizioni dell’eventuale dispensazione del medicinale con onere a carico del Servizio sanitario nazionale;
- tutte le informazioni contenute nella pubblicità devono essere esatte, aggiornate, verificabili e conformi alla documentazione presentata ai fini del rilascio dell’autorizzazione all’immissione in Commercio (AIC) o ai suoi aggiornamenti;
- non sono consentite citazioni che, avulse dal contesto da cui sono tratte, possono risultare parziali o distorsive;
- prima dell’inizio della campagna pubblicitaria, questa deve essere depositata presso l’Ufficio Informazione Scientifica dell’AIFA, e la data di deposito deve essere indicata nel MP divulgato.
Tra gli argomenti di maggior rilievo discussi all’interno del GdL rientrano il deposito dei MP, la loro gestione e l’aumentata tendenza di dinieghi o richieste di integrazione ricevute da parte di AIFA.
Proprio dall’incremento del numero di dinieghi e integrazioni è nata l’idea di quantificare l’impatto che la gestione dei depositi in AIFA dei MP ha sull’attività delle aziende e dell’AIFA stessa, prendendo in esame le varie casistiche ad essi correlate, allo scopo di poter analizzare i risultati e proporre eventuali azioni migliorative congiunte. Tutto questo è stato tradotto nella creazione di un questionario distribuito a tutti i partecipanti del gruppo di lavoro.
- MATERIALI E METODI
Il questionario è stato inviato tramite piattaforma Google Forms ai membri del GdL, è stata inoltre data la possibilità di rispondere tramite un questionario cartaceo ove richiesto.
I quesiti proposti sono stati suddivisi in 8 categorie di motivazioni che portavano ad un diniego o ad una richiesta di integrazione:
- Requisiti formali e di legge (che include, a titolo esemplificativo: erronea apposizione del Codice materiale, della data deposito, dei requisiti di prezzo e classificazione)
- Assemblaggio pratica nel Front End (che include, a titolo esemplificativo: erronea inclusione di allegati alla pratica, loro errato posizionamento nella pratica, descrizione del materiale non esaustiva)
- Problematiche correlate alla natura digitale del MP (che include, a titolo esemplificativo: presenza nel MP di link attivi, canali di distribuzione non corretti)
- Problematiche relative a MP digitale composto da più elementi (che include, a titolo esemplificativo: presenza di elementi promozionali e non promozionali, deposito di pagina sito web in tempi diversi)
- Problematiche correlate a MP cartaceo (che include, a titolo esemplificativo: inclusione non corretta del RCP, utilizzo del QR code per RCP)
- Problematiche relative a MP cartaceo composto da più elementi (che include, a titolo esemplificativo: presenza di elementi promozionali e non promozionali)
- Problematiche relative ai contenuti scientifici (che include, a titolo esemplificativo: claim non sostenuto da un opportuno riferimento bibliografico)
- Altro, nel caso in cui il motivo di richiesta di integrazione o diniego non era riconducibile alle altre categorie
Le categorie sopracitate sono state raggruppate, ai fini della discussione dei risultati (vedere paragrafo 3), in 5 macrocategorie sotto riportate:
- Requisiti amministrativi (che include i punti 1 e 2 sopra: Requisiti formali di legge e Assemblaggio pratica in FrontEnd)
- Problematiche correlate alla Natura digitale del MP (che include i punti 3 e 4 sopra: Problematiche correlate alla Natura digitale del MP e Problematiche relative a MP digitale composto da più elementi)
- Problematiche correlate a MP cartaceo (che include i punti 5 e 6 sopra: Problematiche correlate a MP cartaceo e Problematiche correlate a MP cartaceo composto da più elementi)
- Problematiche relative a contenuti scientifici
- Altro
Il questionario si riferiva a 2 semestri: luglio 2020 – dicembre 2020 e gennaio 2021 – giugno 2021, coprendo di fatto anche parte del periodo pandemico.
- SINTESI DEI RISULTATI
La survey ha ricevuto riscontro da 29 aziende su un totale di 58 società afferenti al GdL. Due aziende hanno utilizzato il formato cartaceo del questionario.
Riportiamo qui di seguito i risultati emersi.
- INTEGRAZIONI
In questo paragrafo sono descritte e valutate le casistiche relative alle integrazioni nei due semestri di riferimento.
Nel primo semestre analizzato (luglio 2020 – dicembre 2020), su 1.910 depositi effettuati sono state registrate 123 richieste di integrazione da parte di AIFA (6,4% del totale di pratiche depositate), di cui 5 hanno successivamente ricevuto un esito negativo (4% del totale delle pratiche integrate).
Nel secondo semestre analizzato (gennaio 2021 – giugno 2021), su 1.931 depositi effettuati sono state registrate 188 richieste di integrazione da parte di AIFA (9,7% del totale di pratiche depositate), di cui 27 hanno successivamente ricevuto un esito negativo (14% del totale delle pratiche integrate).
Pur avendo una numerica ridotta possiamo evidenziare una tendenza in aumento del numero di richieste di integrazione da parte di AIFA e un incremento degli esiti negativi a seguito dell’integrazione da parte delle aziende.
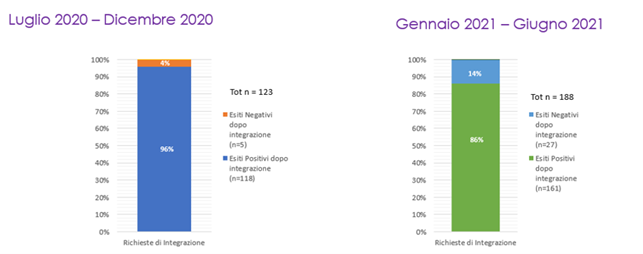
Figura 1 – Richieste di integrazione ed esiti delle pratiche nei periodi analizzati
Nel primo semestre analizzato (luglio 2020 – dicembre 2020), il 66% delle integrazioni è dovuto a motivi amministrativi, il 19% a problematiche correlate alla natura digitale del MP, il 5% a problematiche correlate alla natura cartacea del MP e solo il 2% a tematiche correlate ai contenuti scientifici.
Nel secondo semestre (gennaio 2021 – giugno 2021), il 51% delle integrazioni è dovuto a motivi amministrativi, il 37% a problematiche correlate alla natura digitale del MP, il 7% a problematiche correlate alla natura cartacea del MP e solo il 2% a tematiche correlate ai contenuti scientifici.
È interessante notare che sono emerse alcune richieste da parte di AIFA non riconducibili alle classi precedentemente individuate che sono state raggruppate nella categoria “Altro”. Tra queste citiamo alcuni esempi da tenere in considerazione nell’ambito della revisione interna dei materiali aziendali:
- documentare l’autorizzazione all’uso dei loghi presenti nel MP (esempio: Logo di Società Scientifiche o Regioni);
- aggiunta di un wording per specificare che il mezzo non è rivolto ai pazienti;
- richiesta di inserimento dei requisiti di legge relativi a tutti i medicinali presenti in un MP multibrand.
In sintesi, da una lettura congiunta dei risultati relativi ad entrambi i semestri, possiamo evidenziare che delle integrazioni ricevute:
- 1 su 2 è dovuta a motivi amministrativi;
- aumenta nel tempo la richiesta di integrazioni dovuta a problematiche digitali;
- i contenuti scientifici hanno un rilievo marginale.
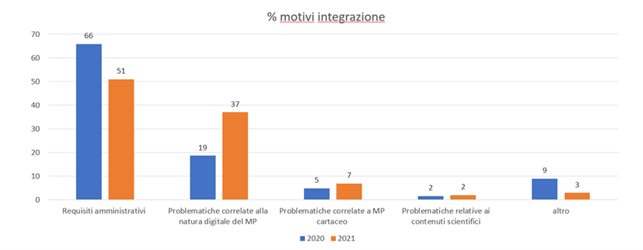
Figura 2 – Motivazioni delle richieste di integrazione nei periodi analizzati
b. DINIEGHI
Nel primo semestre analizzato (luglio 2020 – dicembre 2020), su 1.910 depositi, 149 pratiche hanno avuto esito negativo, corrispondente a circa l’8% del totale di pratiche depositate. Nel semestre successivo (gennaio 2021 – giugno 2021), la percentuale sale al 10% (188 pratiche con esito negativo rispetto a un totale di 1.931 pratiche depositate).
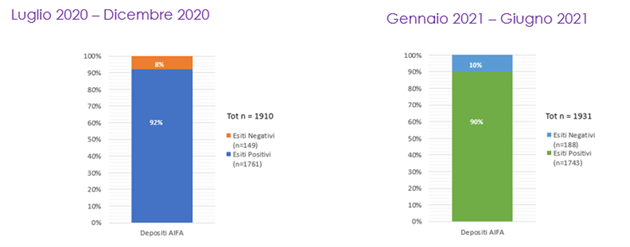
Figura 3 – Dinieghi ricevuti al deposito iniziale delle pratiche nei periodi analizzati
In entrambi i semestri analizzati, la maggior parte dei dinieghi (48% nel 2020 vs 65% nel 2021) è da attribuirsi a:
- l’inadempienza rispetto ai requisiti formali di legge, ivi compresi:
- la mancanza o l’erronea attribuzione del codice di deposito,
- la mancanza del prezzo,
- assenza del RCP;
- l’assemblaggio del MP in AIFA Front End;
- le incomprensioni tra l’azienda e l’Autorità in merito alla spiegazione della composizione del MP.
La seconda causa di diniego più frequente è relativa alla natura digitale del MP e alle commistioni, sempre in ambito digitale, di contenuti promozionali e non promozionali, che rappresenta il 32% nel 2020 e il 35% dei casi nel 2020 e 2021 rispettivamente.
I dinieghi associati a mezzi promozionali cartacei rappresentano il 15% e 23% negli anni 2020 e 2021. I dinieghi correlati alla valutazione del contenuto scientifico del MP sono, per entrambi i semestri, trascurabili e nell’ordine del 1%.
Alcuni dinieghi, classificati nella categoria “Altro”, non rientrano in alcuna delle categorie sopra descritte, ma sono di interessante rilevazione poiché relativi alla commistione di pubblicità sanitaria con altri elementi, quali materiali educazionali o materiali per il paziente.
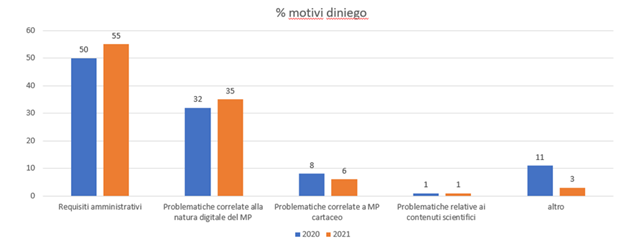
Figura 4 – Motivazioni dei dinieghi ricevuti nei periodi analizzati
- CONSIDERAZIONI
Nell’analisi delle motivazioni che possono determinare un diniego o richiesta di integrazione ci si è chiesti perché la percentuale di dinieghi/integrazioni amministravi è così alta. Alcuni errori possono derivare da una difficoltà da parte delle aziende nella gestione dei requisiti obbligatori di legge. Si evidenziano a titolo esemplificativo l’assenza o non correttezza di codice materiale, data di deposito, prezzo e classificazione, RCP. Tali requisiti, seppur ben noti da parte degli addetti ai lavori, spesso possono essere gestiti dalle aziende in modo non conforme alle attese di AIFA. È pur vero che non sempre è possibile reperire le linee guida aggiornate, poiché talvolta queste non sono pubblicamente condivise. Inoltre, la continua evoluzione dei MP in ambito digitale rende alle volte difficile individuare le regole pertinenti al MP che si intende proporre.
A tal proposito emerge dall’analisi che un diniego/integrazione su tre è correlato alla natura digitale del mezzo. Se da un lato è evidente che è aumentato il numero dei depositi di MP di natura digitale, in accordo allo sviluppo di nuove tecnologie e come conseguenza della pandemia di Covid 19, dall’altro non sono state parimenti aggiornate regole e/o linee guida che tengano conto di queste nuove modalità di comunicazione. Il risultato è che a volte appare difficile adattare i requisiti normativi in vigore perché spesso non abbastanza flessibili da ricomprendere le casistiche derivanti dallo sviluppo di MP di natura digitale.
Un dato positivo da evidenziare è la percentuale limitata di dinieghi/integrazioni di MP di natura cartacea. L’esperienza acquisita negli anni da parte delle aziende e la collaborazione dell’Autorità potrebbe aver favorito il raggiungimento di questo risultato.
In ultimo emerge che le problematiche derivanti dall’analisi dei contenuti scientifici dei MP notificati costituiscono un dato marginale.
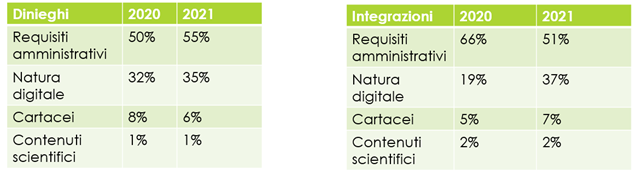
Figura 5 – Sintesi di Dinieghi ed integrazioni
Una delle conseguenze di quanto sopra descritto è un aumento del carico di lavoro dovuto alla rilavorazione dei MP da parte delle Aziende e un contestuale aumento dell’attività di verifica da parte dell’Autorità.
Dalla survey emerge che la percentuale di MP da rimettere in lavorazione, a causa di dinieghi o richieste di integrazione, è pari al 14,2% nel 2020 e al 19,4% nel 2021 sul totale dei depositi effettuati. Si evidenzia quindi che nel 2021 1 MP su 5 richiede una nuova lavorazione da parte dell’Azienda e quindi un’ulteriore revisione da parte dell’Autorità.
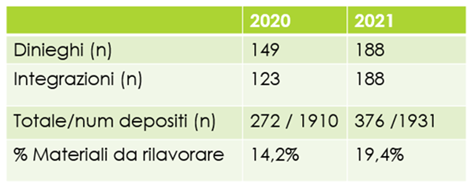
Figura 6 – Analisi dei materiali da rimettere in lavorazione
- TIP & TRICKS
Di seguito riportiamo alcuni esempi pratici di MP che auspichiamo possano essere utili per facilitare l’esito positivo del deposito, riducendo il rischio di incorrere in richieste di integrazioni o dinieghi da parte dell’Autorità. L’approfondimento sotto riportato si riferisce ai siti internet aziendali, ed in particolare alla parte ristretta relativa ai medicinali di cui l’azienda è titolare destinata agli operatori sanitari, che deve essere depositata in AIFA come materiale di informazione medico-scientifica. Trattasi di casi molto comuni per le aziende farmaceutiche, ma complessi per la loro natura stessa. All’interno della stessa pagina internet possono essere presenti tante tipologie diverse di MP (esempio slide deck, e-reprint, podcast, video).
Ad oggi AIFA considera il sito web come un contenitore di differenti MP depositati singolarmente, ciascuno con il proprio codice e data di deposito. Questa soluzione rappresenta un nuovo approccio da parte dell’Autorità per far fronte all’aumentato numero e complessità dei MP ricevuti. Infatti, nelle prime esperienze di deposito l’Ufficio Informazione Scientifica di AIFA aveva considerato il sito web come un unico MP in cui tutti i contenuti dovevano riportare lo stesso codice e data di deposito, in linea con quanto ancora previsto per i MP cartacei.
| TIP &TRICKS
SITO WEB AZIENDALE – CONTENUTI PROMOZIONALI DESTINATI ALL’OPERATORE SANITARIO Caratteristiche necessarie:
Ulteriori dettagli: Su una stessa pagina promozionale del sito web possono essere presenti diverse tipologie di MP da depositare contestualmente o già precedentemente depositati in AIFA. Su ogni MP devono essere presenti tutti gli elementi obbligatori di cui sopra.
Casi particolari:
|
- CONCLUSIONI
Gli ultimi due anni sono stati caratterizzati da un massivo ricorso a MP digitali e a forme alternative alla visita face to face per le attività promozionali, dovuti anche agli effetti della pandemia di Covid-19.
Le nuove modalità di promozione hanno certamente sfidato una normativa già di per sé obsoleta, evidenziando un cambio di passo che, se prima era solo ravvisabile, oggi è concretamente necessario. Lo sforzo da ambo le parti è diventato una necessità finalizzata anche ad una razionalizzazione delle attività e delle risorse, sia da parte del professionista regolatorio dell’Azienda farmaceutica, che deve ispirare il dialogo con AIFA, che da parte dell’Autorità competente che deve aprire le porte a questa interazione. La Survey descritta nell’articolo evidenzia che le non conformità dei MP potrebbero essere risolvibili con maggiore attenzione agli adempimenti dei requisiti di legge da parte delle aziende. Di contro, la sempre maggior complessità dell’ambiente digitale e dei materiali che in esso sono gestiti rende necessario un maggiore dialogo tra le parti per facilitare la comunicazione e promuovere l’evoluzione dei sistemi amministrativi, agevolando le attività degli uffici competenti.
Per rendere omogenea la revisione degli uffici regolatori delle aziende e dell’Autorità competente, ad oggi certamente sarebbe ravvisabile una proficua interazione per il tramite delle associazioni di categoria al fine di promulgare delle Q&A dedicate alle più frequenti problematiche emerse negli ultimi anni, in primis quelle digitali, che siano univoche ed accessibili. Inoltre sarebbe auspicabile la pubblicazione delle “Linee guida sulla pubblicità dei medicinali presso gli operatori sanitari”, come previsto dall’art 119 del D.Lvo 219/06, ed in linea con quanto emerge dal Piano Integrato di Attività e Organizzazione (PIAO) 2022 – 2024 rilasciato dall’AIFA il 20/4/2022.
In fase di pubblicazione di questo articolo, AIFA ha inviato ad alcune aziende, in allegato alle richieste di integrazione o verifica negativa, un documento denominato “Domande & Risposte attinenti al Servizio Online “IMS – Informatori Scientifici” e alle questioni pertinenti alla relativa materia” datato 15 settembre 2022. Questo documento, che annulla e sostituisce gli analoghi pubblicati sul Portale AIFA in data 10 febbraio 2013 e 22 Giugno 2016, riporta chiarimenti sulla pubblicità dei medicinali presso gli operatori sanitari. Si ravvisa quindi l’impegno dell’Autorità ad identificare uno strumento di comunicazione con le Aziende che possa essere fruibile da tutti gli attori coinvolti nella gestione dei materiali promozionali.

